CURE8
A New Level of Medical Image Data Management
What happens when you combine cutting-edge technologies from big data sectors like retail and automotive with EXINI’s assets and experience in medical imaging? The answer is CURE8 – a cloud-based application created from scratch for large-scale image transfer and management, as well as a digital ecosystem for building secure and compliant applications quickly and with confidence.
CURE8 for Clinical Trials
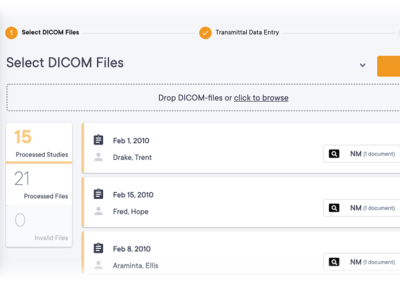
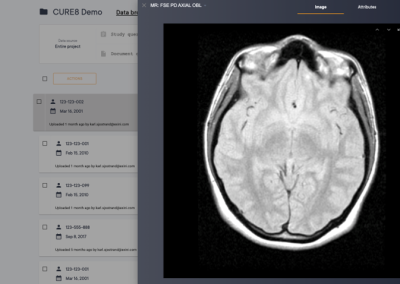
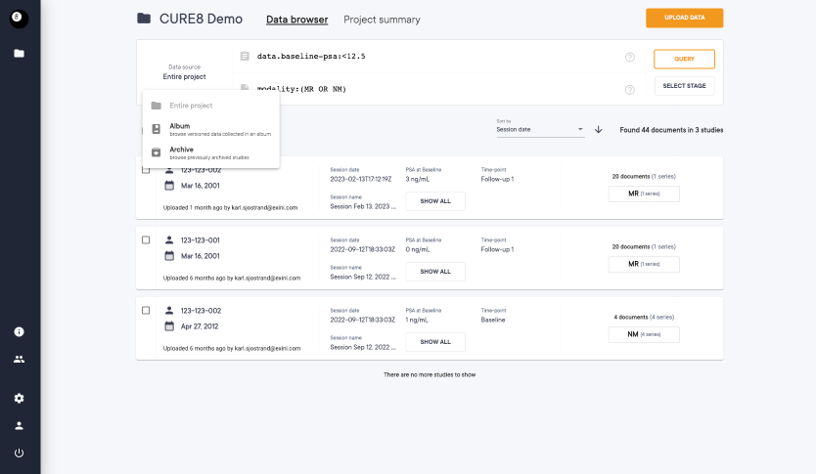
CURE8 provides a browser-based user interface for image transfer, storage, sharing and powerful management. Customization is a core principle of CURE8 making it possible to create tailored workflow and external application integrations to cater to the specific needs of a clinical trial. Out of the box, CURE8 integrates seamlessly with EXINI’s imaging biomarker solutions.
CURE8 for Research
Leading academic institutions world-wide are using CURE8 to facilitate image collection, sharing, analysis, and disseminating results. Reproducible research is supported by maintaining an audit trail of user actions and full version history of data. Results are associated with a cohort of data at a point in time and can be revisited or recreated, or used as a basis for new analyses. Industry-standard and compliant tools for de-identification, user access control, and secure transfer and storage provide confidence in handling sensitive datasets.
CURE8 for Developers
Don’t reinvent the wheel and avoid implementing your own standards for security and privacy. Focus on the application, not the supporting infrastructure. These are lessons learned the hard way over EXINI’s past. CURE8 was in part created to make it possible for EXINI to develop and maintain a large number of applications, all sharing a common technology platform. We are now offering these same benefits to companies wanting to build powerful and robust applications with proven integrations into clinical workflows.
Find out More
We would love to tell you more about CURE8 and to understand your use cases!
Don’t hesitate to contact us for a demo and discussion.
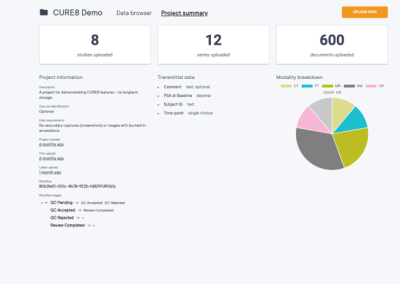
Foundations of CURE8
- Users work in teams
Data is private to a team - Work & data is divided into projects
Each project specifies what data to collect - Albums work just like photo albums, they form named and versioned subsets of data
Can collect data across projects, Can be shared with other teams - Workflows specify stages that data can belong to and move between
Use Cases
- Collect PSMA PET/CT data from 10 sites with de-identification of protected health information. Keep sites’ data private and separate, with aggregation of all project data into a coordinator account where data management and reconciliation takes place.
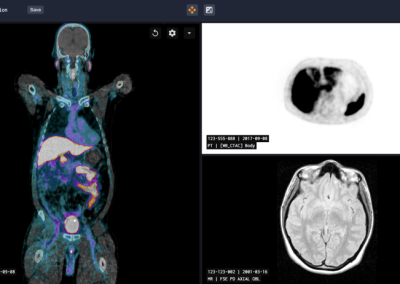
- Allow limited access for three independent image readers, using aPROMISE to quantify scans accurately and reproducibly. Coordinators monitor a live feed of reader progress.
- Export comprehensive quantitative results for statistical analysis or use CURE8’s extensive programming toolkits for running the analysis directly on the platform.
Large-scale image transfer and management
- Clinical Trials
- Research
- Developers